|
| |

Suponhamos
agora uma soluçăo de um ácido, uma base ou um sal em água,
por exemplo, cloreto de sódio em água. Sabemos que suas
moléculas se dissociam, isto é, existem íons de sódio e
de cloro soltos na água, caminhando em direçőes quaisquer.
Suponhamos que nessa soluçăo sejam mergulhadas duas placas
metálicas A e B, ligadas aos polos de um gerador G, que
pode ser um acumulador ou uma série de pilhas que deęm mais
ou menos 6 volts (fig. 197). As duas placas metálicas săo chamadas
eletrodos. O eletrodo negativo, isto é, aquele ligado ao
polo negativo do gerador é chamado cátodo. O eletrodo positivo,
isto é, aquele ligado ao polo positivo do gerador é chamado
anodo.
O mecanismo
da conduçăo da eletricidade pelos eletrólitos é explicado
do seguinte modo: Ao dissolvermos o ácido, a base ou o
sal na água, há dissociaçăo de moléculas do ácido, da base
ou do sal, e os íons resultantes ficam vagando pela soluçăo.
Depois, quando introduzimos na soluçăo os eletrodos ligados
aos polos do gerador, como há diferença de potencial entre
eles, forma-se um campo elétrico
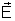 entre os eletrodos, dirigido do anodo (
entre os eletrodos, dirigido do anodo (
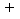 ) para o cátodo (
) para o cátodo (
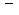 ).
).
|
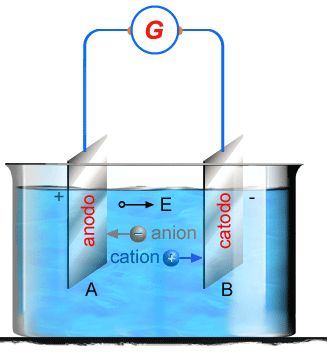 Figura 197 Figura 197 |
Por
causa desse campo os íons ficam sujeitos a forças. Os íons positivos
ficam sujeitos ŕ forças que tem o mesmo sentido que o campo, e os
negativos, ŕ forças que tem sentido oposto ao do campo. Em virtude
dessas forças os íons deixam de vagar pela soluçăo sem direçăo determinada,
mas, săo “dirigidos”: os cátions săo dirigidos para o cátodo, e
os anions, para o anodo. Forma-se entăo a corrente elétrica.
Já
tínhamos assinalado anteriormente, no tópico "Diferentes
Tipos de Condução" , que num eletrólito a corrente é constituída
pelo movimento de cargas positivas num sentido e de cargas negativas
em sentido oposto, e o número de partículas positivas que se deslocam
num sentido é igual ao número de partículas negativas que se deslocam
no outro. Mas, exclusivamente para raciocínio, podemos imaginar
que em uma corrente seja constituída exclusivamente por partículas
positivas, em número duplo, que se deslocam dentro da soluçăo do
anodo para o cátodo.
Vimos
já que a conduçăo da eletricidade nos metais năo é do
mesmo tipo que nos eletrólitos. Que nos metais ela é constituída
exclusivamente pelo movimento de elétrons, que se deslocam
num só sentido, enquanto que nos eletrólitos é constituída
pelo movimento de íons positivos num sentido e de íons negativos
em sentido oposto. Ora, quando fazemos passar corrente
por um eletrólito, os eletrodos săo ligados ao gerador G
por fios metálicos a e b. Vejamos, entăo, como se explica
a corrente elétrica nesse circuito fechado, pois nos metais
a e b a corrente é constituída pelo movimento de elétrons,
e na soluçăo, pelo movimento de íons (fig. 198). O que se passa é
o seguinte:
O íon
negativo tem elétrons a mais, e é atraído pelo anodo, que
é positivo; ao chegar ao anodo ele cede os elétrons que
tem a mais e se transforma num átomo neutro. Os elétrons
cedidos ao anodo, ęste os envia ao fio metálico a, que conduz
esses elétrons do anodo para o gerador. O gerador envia
esses elétrons ao cátodo, através do fio metálico b. (O
cátodo é negativo porque recebe elétrons). O íon positivo
tem falta de elétrons, e é atraído pelo cátodo; ao chegar
aí, retira elétrons, e se transforma em átomo neutro.
|
 Figura 198 Figura 198 |
Em
resumo: por fora da soluçăo, nos fios metálicos a e b que ligam
os eletrodos ao gerador, a corrente é constituída pelo movimento
de elétrons, que se dirigem do anodo para o cátodo através do gerador;
esses elétrons săo retirados dos anions pelo anodo e cedidos aos
cátions pelo cátodo.

Suponhamos
a conduçăo da eletricidade por uma soluçăo de cloreto de sódio.
As moléculas se dissociam em íons de sódio (positivos) e íons
de cloro (negativos). O íon de cloro, que é um átomo de cloro
com um elétron a mais, ao chegar ao anodo cede a ele esse
elétron e se torna um átomo de cloro (neutro); o elétron cedido
ao anodo, ęste o manda ao gerador. O íon de sódio, que é
um átomo de sódio com um elétron a menos, ao chegar ao cátodo
retira um elétron dele e se torna um átomo de sódio (neutro);
esse elétron foi fornecido ao cátodo pelo gerador (fig. 199). |
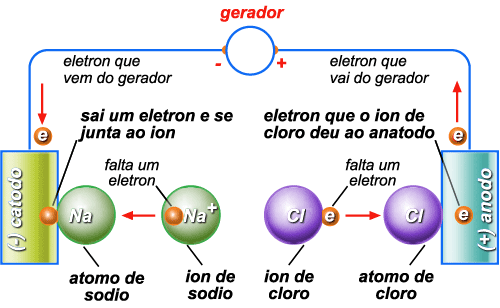
Figura 199
|
|
|